

Parole chiave: monomero
Questa pagina è dedicata
ad una piccola introduzione su come vengono prodotti i polimeri. Una reazione
chimica che da origine ai polimeri viene detta polimerizzazione Ci sono
molti tipi di reazioni come queste. Tutte le polimerizzazioni hanno una
cosa in comune. Iniziano tutte con piccole molecole e si uniscono per formare
molecole giganti. La piccola molecola originaria viene detta monomero.
Si possono unire in vari modi. La gente ama categorizzare le cose, così
ci dice E.Kant, e le reazioni di polimerizzazione non sono escluse dal
nostro bisogno di classificazione.
Non elencheremo ancora queste classificazioni
Presentarsi solo con alcune
categorie non è sufficiente per noi. Dobbiamo elencare diversi sistemi
di classificazione. I diversi sistemi possono spesso creare confusione.
Cerchiamo di chiarirli il più possibile elencando i diversi sistemi.
Il primo sistema è quello della Addizione-Condensazione ideata da
Charters.
Questo sistema divide in
due tipi la polimerizzazione e se siete veramente intelligenti avrete sicuramente
capito che questi due tipi di polimerizzazione sono:
polimerizzazione per addizione o poliaddizione
e
polimerizzazione per condensazione o policondensazione
Viene detta polimerizzazione per addizione la polimerizzazione in cui tutta la molecola di monomero diventa parte del polimero. Viene detta polimerizzazione per condensazione la polimerizzazione in cui una parte della molecola di monomero viene eliminata quando il monomero diventa parte del polimero. La parte che viene eliminata è di solito una molecola piccola come l'acqua, o HCl. Vediamo qualche esempio per illustrare il tutto.
Quando l'etilene è polimerizzato per produrre il polietilene, ogni atomo della molecola di etilene diventa parte del polimero. Il monomero viene addizionato interamente al polimero. Si può dire che un polimero di addizione è come un buon amico che accetta tutto di te, i pregi e i difetti.
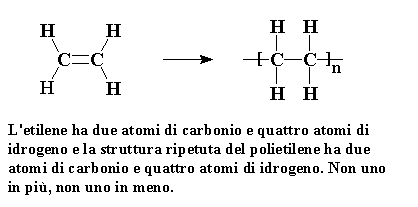
L'etilene ha due atomi di carbonio e quattro atomi di idrogeno e la struttura ripetuta del polietilene ha due atomi di carbonio e quattro atomi di idrogeno. Non uno in più, non uno in meno.
Un
polimero di condensazione è simile ad un altezzoso circolo che dice
"Certamente puoi far parte del nostro club ma solo se eviti quei tuoi amici"
Vedete in una polimerizzazione per condensazione alcuni atomi del monomero
non finiscono nel polimero. Quando il nylon 6.6
si ottiene con il cloruro di adipoile e la esametilendiammina, atomi
di cloro del cloruro di adipoile, insieme ad atomi di idrogeno amminico,
vengono espulsi sotto forma di HCl.

Questo atomo di cloro e questo atomo di idrogeno non terminano nel polimero. Si staccano per formare HCl
La linea finale
Volete la versione abbreviata? La polimerizzazione per condensazione rilascia sottoprodotti. La polimerizzazione per addizione, no.
Parliamo ora del prossimo
sistema di classificazione ideata da Flory: la polimerizzazione a catena
ed a stadi
La polimerizzazione
a catena ed a stadi
L'altro sistema di classificazione per la polimerizzazione divide questo tipo di reazione in due categorie che sono:
polimerizzazione a catena
e
polimerizzazione a stadi
Molto bene. Ora la differenza tra una polimerizzazione a catena ed una polimerizzazione a stadi è leggermente più complicata della differenza tra una polimerizzazione per addizione ed una polimerizzazione per condensazione. Si può definire così:
In una polimerizzazione a catena, i monomeri diventano parte del polimero simultaneamente. Semplice, vero? Per farvi vedere come avviene ecco una figura di una polimerizzazione a catena, in pratica una polimerizzazione anionica dello stirene per formare il polistirene. Date un'occhiata.
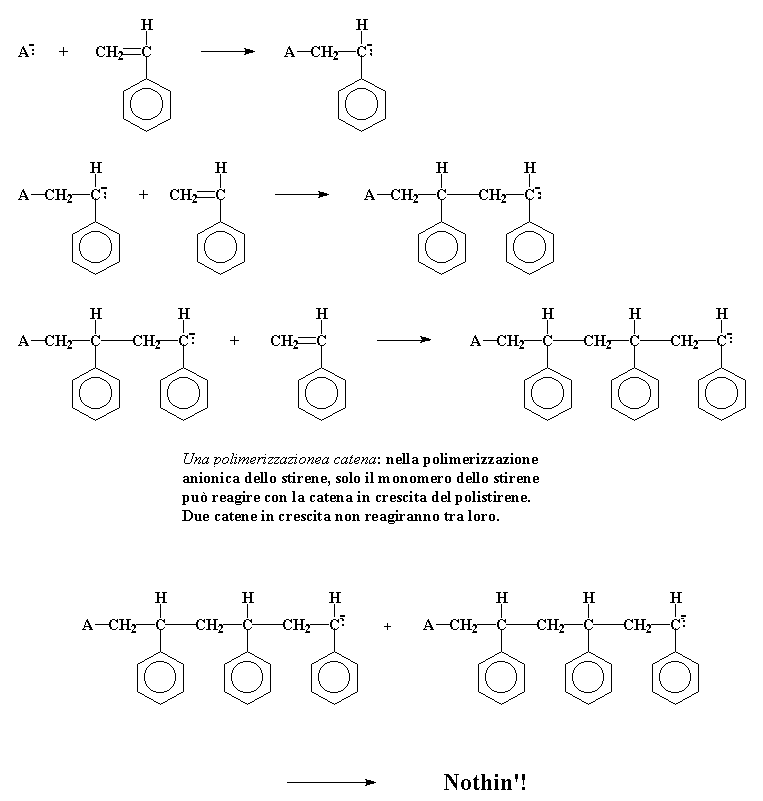
Nella polimerizzazione a stadi, le cose sono più complicate. Diamo un'occhiata alla polimerizzazione a stadi di due monomeri, il cloruro dell'acideo tereftalico e l'etilenglicole, per ottenere un poliestere denominato polietilenterftalato. Prima di tutto i due monomeri reagiranno per formare un dimero. Sembra abbastanza semplice.

Il cloruro dell'acido tereftalico e l'etilenglicole reagiscono per formare un dimero estere
A questo
punto in una polimerizzazione a catena, può accadere solo una cosa:
un terzo monomero si aggiunge al dimero per formare un trimero poi un quarto
per formare un tetramero e così via. Ma qui nella terra libera della
polimerizzazione a stadi questo dimero può comportarsi in molti
modi differenti. Può, naturalmente, reagire con uno dei monomeri
per formare un trimero:
Il nostro piccolo dimero può reagire con una molecola del cloruro dell'acido tereftalico......

...o può reagire con una molecola di etilenglicole
Ma può fare anche altre cose. Può reagire con un altro dimero per formare un tetramero

Può persino diventare matto e ragire con un trimero per formare un pentamero.

La mania della fusione
!
Il dimero si unisce al
trimero per formare un pentamero. Potrà terminare questa pazzia?
Pensate al modo in cui la vostra banca si unisce ad altre banche e diventa sempre più grande e avrete un'idea di ciò che succede.
La linea finale
La differenza principale è questa: in una reazione a stadi, le catene in crescita possono reagire una con l'altra per formare catene ancora più lunghe. Ciò è valido per catene di ogni lunghezza. Il monomero o dimero può reagire nello stesso modo in cui agisce un monomero con una catena formata da centinaia di unità. Nella polimerizzazione per addizione, solo i monomeri possono reagire con le catene in crescita. Due catene in crescita non si possono unire nel modo in cui si uniscono in una polimerizzazione a catena.
Differenze inconciliabili
Sono sicuro che molti di voi, brillanti studenti, hanno notato che la nostra polimerizzazione a stadi per ottenere un poliestere ha dato origine ad un sottoprodotto, HCl. Sarà quindi una polimerizzazione per condensazione oltre ad essere una polimerizzazione a stadi.
Avrete anche notato che la nostra polimerizzazione a catena dello stirene non ha generato sottoprodotti. Effettivamente si tratta di una polimerizzazione per addizione oltre ad essere una polimerizzazione a catena.
E' facile concludere che una polimerizzazione a stadi ed una polimerizzazione per condensazione sono la stessa cosa, così pure sono la stessa cosa una polimerizzazione a catena ed una polimerizzazione per addizione. Ma non è sempre così. Ci sono polimerizzazioni per addizione che sono polimerizzazioni a stadi. Un esempio è la polimerizzazioneche produce poliuretani. Esistono anche polimerizzazioni per condensazione che sono polimerizzazione a catena. Cercare di riconciliare il sistema di classificazione della crescita a catena-crescita a stadi ed il sistema di classificazione addizione-condensazione è solo una perdita di tempo Ogni sistema ha i suoi criteri, e le distinzioni fatte per un sistema non sempre sono le stesse distinzioni fatte per l'altro.
Non cercate quindi di riconciliare
i due sistemi. Sappiate solo che le polimerizzazioni possono essere a catena
o a stadi e possono essere per condensazione o per addizione.